
QINMS.com || 首页 ||
EP9-A2主要是为临床实验室和诊断试剂、仪器制造商用来评价测定同一物质的两种方法之间的偏倚,在理想状态下待评方法应该和参考方法进行比较,但一般情况下做不到,现主要还是用作评价两种方法得到相应的结果是否在实验统计学的范围之内,新方法是否能够替代原有的方法,新进的试剂、仪器能否和之前使用的是否在同样的水平上。若制造商也依据EP9-A2提供了实验数据,或者临床实验使用相同的参比方法,临床实验室还而已用来和厂商的声明做比较,以确定其性能是否可以接受。
1 评价一个分析方法需要的条件:
1.1操作者要有足够的时间熟悉仪器操作和保养程序;
1.2 操作者要有足够的时间来熟悉评价方案;
1.3评价实验过程中,两种方法都必须有适当的质量控制;
1.4 两种方法必须要有足够的数据以保证结果有代表性。
一般建议至少在5个工作日内最少要分析完40份患者样本。在遵循厂家的推荐进行校准的条件下,增加测定样本数及测定天数,可以提高实验的可靠性及有效性。
用待评方法和参比方法对每一患者样本各作两份测定。分析每一方法在同一批内的双份测定结果。应尽可能使至少50%样本的测定结果处于实验室的参考区间之外。
2. 一些定义
分析测定范围(AMR):一种方法能直接测量无稀释或浓缩样本的分析值范围。
偏倚:预期测定值和真值的差值。
临床可报告范围(CCR):一种方法能定量报告的分析值范围,允许标本稀释、浓缩或通过其他预处理延伸直接测定范围。
相关系数(r):两个随机变量协方差和其标准差的比率。
Deming 回归:根据方法比较实验中两方法的允许测定误差评估斜率和截距参数的一种方法,每种方法的测定误差均用于评估程序。
待测物:一种待测量的物质。
Passing-Bablok:根据方法比较实验中使用非参数程序评估斜率和截距参数的一种方法。
真值:多次重复测量结果的均值与可接受参考值间的符合程度。(注:真值的测量通常用偏倚表示。
医学决定水平(MDL):指在诊断及治疗工作时,对疾病诊断或治疗起关键作用的某一被测成分的浓度,临床上必须采取措施的检测水平。
3.方法对比试验:
3.1 患者样本的收集和处理可以按照实验室的操作规范和制造商的推荐办法,样本尽量用当天的,避免储存,没法避免时由待测物的稳定性来决定储存时间和条件,实验过程拒收某一样本时,要做好记录,说明拒收原因。样本数量至少是40份,可根据实际增加数量,样本量要充足,至少保证能用两种方法均进行双份测试后还有剩余,以备后续可能的追踪实验等。样本量实在不足时,可将适当的两个样本混合当一个样本用,混合的前提是两个样本患者的病史相同,待测物浓度接近,若样本是全血,混合还要考虑血清配型等问题(所以非不得已,最好别混)。
3.2 参比方法:
参比方法可以是实验室当前使用的方法、生产厂商声明的方法或者是参考方法等。作为参比方法应达到以下几点要求:
3.2.1 具有比待测方法更好的精密度;
3.2.2 尽可能不受已知干扰物的干扰;
3.2.3 和待评方法的单位一致。
3.2.4可溯源性。
本实验并不能将不同来源的误差归咎于被比较的每一方法。(可参见NCCLS EP14 基质效应的评价)干扰可能与精密度一样影响两方法间测定结果的差值。(可参见 NCCLS EP7 临床化学实验干扰 提议指南)
3.3 测定范围
应在由临床意义的范围内,例如医学决定水平范围内评价待评方法,通常样本在参考范围两边都有分布,分析物浓度在测定范围内尽可能均匀分布,分析测定范围是制造商提供、声明的分析浓度区间。(部分项目可参照原文件提供的表1a和1b的推荐范围)。
3.4 样本的测定:
3.4.1 样本的双份测定,应指定第一次测定的顺序,然后按反向顺序检测第二次,顺序中样本的浓度应尽可能随机排列。例如 按照编号1、2、3、4、5、6、7、8和8、7、6、5、4、3、2、1顺序来进行双份测试,两种方法测试步骤应一样,但每种方法可以有不同的开始顺序。
3.4.2 对于一个给定的样本,参比方法和待评方法均应在分析物浓度稳定的时间内测试,并且全部的样本应在2个小时内测完。
3.4.3 若方法学对比试验是在精密度试验完成时候进行(精密度试验可参考 NCCLS EP5,临床化学设备操作精密度评价),一天最多可测定8个样本(40个样本就用5天);若是同时进行着两个试验,每天就只能测试4个样本,这样的话约在10-15天内完成,将患者样本分布在多一点的天数和批次上测试,也是较适宜的。
3.5 数据收集过程的检查。
3.5.1 分析系统误差:出现时,做记录,最后数据分析时剔除。
3.5.2 人为误差:做记录,最后数据分析时剔除。
3.5.3 其他数据不一致(没查出原因的双份数据不一致):做记录,并保留原始数据最后做离群值检验来决定去留。
3.6实验中应遵循实验室和/或制造商的常规质量控制程序。保留质控图,任一方法出现失控时应重新测定,直到达到要求的样本数为止
3.7实验过程任何需要删除的数据均应仔细形成文件并保留,记录所发现的原因和问题。
4. 数据初步分析
4.1 数据检查过程概要
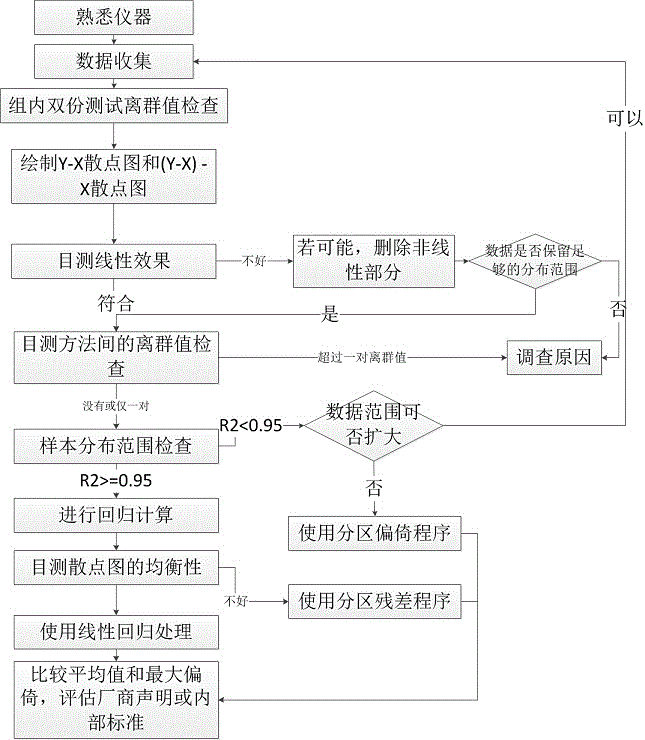
4.2分析过程每一步的逻辑流程图
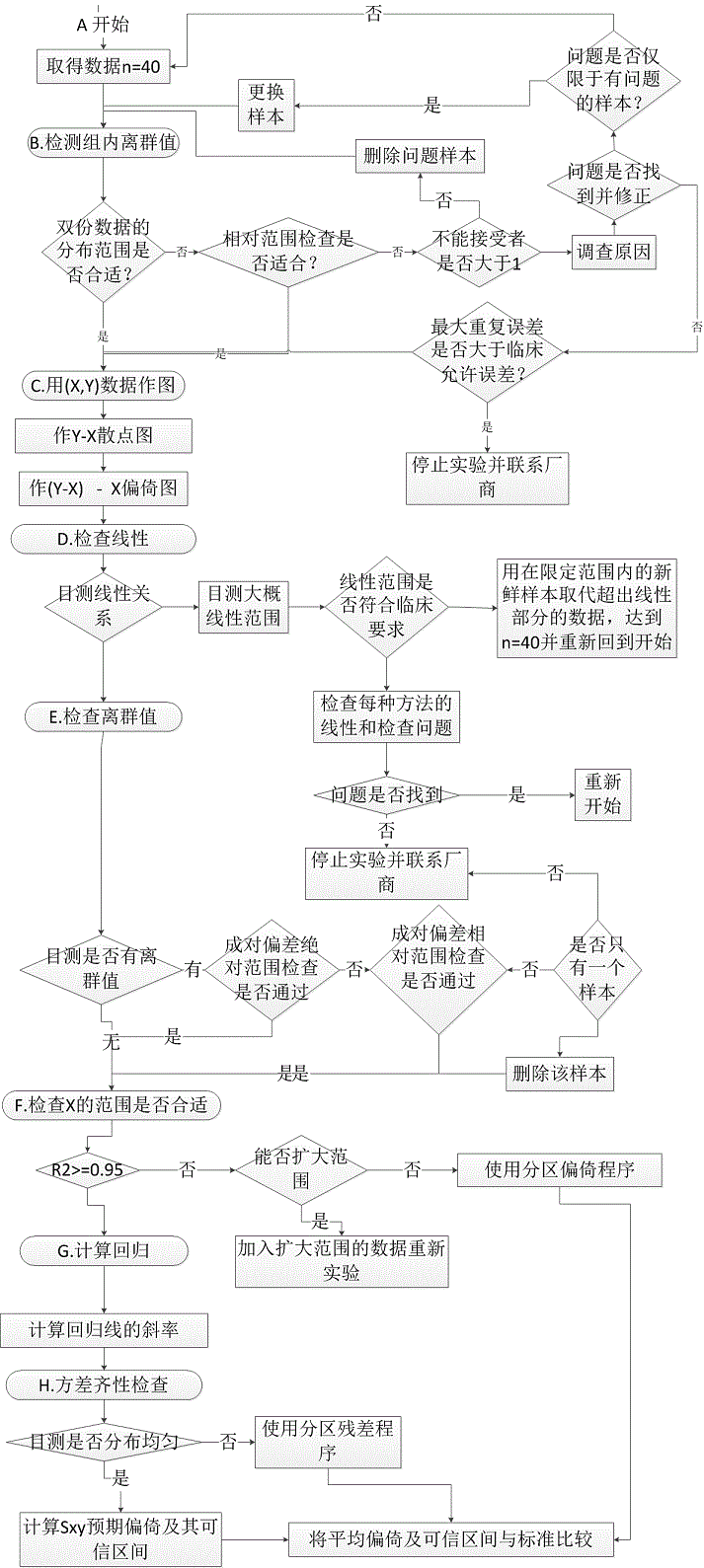
5.数据处理
数据处理是个头疼的问题,在这里就不直接写出来,可直接参照原文件即可;改天想通了,再弄个专门的小软件来处理这些数据,那就方便了。
6.原文下载地址(英文版):点击下载